חוקרים וחוקרות מבית הספר להנדסה מכנית פרסמו מאמר בכתב העת היוקרתי Chemosphere


מחקר
חוקרים וחוקרות מבית הספר להנדסה מכנית פרסמו מאמר בכתב העת היוקרתי Chemosphere

המיקרופלסטיק נמצא כמעט בכל מקום, בקופסאות האוכל ובתרופות שלנו, בגינה הציבורית, בצעצועים של הילדים, בבקבוקי שתיה, בבגדים, במחשבים, בטלפונים הניידים. הם יכולים להיות מסוכנים לבריאות האדם, במיוחד כשהם לא לבדם.
מחקר חדש של המעבדה לננוטכנולוגיה סביבתית בראשות דר' אינס צוקר ובהובלת הדוקטורנט אנדריי איתן רובין מוצא כי מיקרופלסטיקים הם בעלי פוטנציאל לספיחה של חומרים אורגנים רעילים בסביבה הימית.
כשהצמד מגיע לבני האדם, רעילותם של המיקרופלסטיקים יחד עם החומרים הספוחים (אשר אינם רעילים בריכוז שנספח) מוגברת פי 10! תיאור המנגנון לפיו המיקרופלסטיק משמש נשא אפקטיבי של המזהם מהסביבה אל תנאים שמדמים סביבה תאית, ולבסוף גורם לרעילות מוגברת פורסם לאחרונה בכתב העת היוקרתי Chemosphere
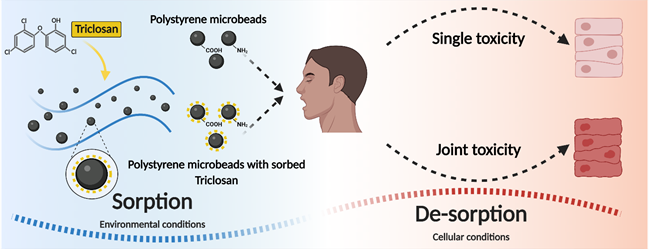
באיור (איור מהמחקר) החוקרים מראים 2 מסלולי חשיפה למיקרופלסטיק, בראשון כשהוא ללא מזהמים ספוחים עליו (נקי) והמסלול השני כשהמיקרופלסטיק ספח מזהם מהסביבה.
"במחקר הזה אנחנו מראים שאפילו ריכוזים מאוד נמוכים של מזהמים סביבתיים, שאינם רעילים לאדם, כאשר הם ספוחים על המיקרופלסטיק גורמים לעלייה ברעילות. הסיבה לכך, היא שבעצם המיקרופלסטיק מהווה מן מגנט למזהמים סביבתיים ומרכז אותם על גביו, הוא "מסיע" אותם דרך מערכת העיכול שלנו ומשחרר אותם בצורה מרוכזת באזורים מסוימים ובכך גורם לרעילות מוגברת. חדשנות המחקר היא בכך, שבעצם בפעם הראשונה אנחנו מראים תמונה כוללת של הגורל המיקרופלסטיק, מרגע השחרור שלו לסביבה, דרך ספיחה של מזהמים סביבתיים ועד לרעילות מוגברת באדם." מסביר אנדריי איתן רובין.
אלה שמתאהבים בבעיה הם אלה שממציאים לה פתרון

מחקר
סטודנטים מתוכנית המצטיינים של הפקולטה להנדסה, בהנחיית ד"ר ביסקר, פיתחו סימולציית מחשב לחיזוי הדינמיקה של מערכות ביולוגיות מחוץ לשיווי משקל תרמודינמי

עדי בן-ארי ולירון בן-ארי הם סטודנטים להנדסת חשמל ופיזיקה, בשנה ד' ובתוכנית המצטיינים של הפקולטה להנדסה. אין זה במקרה שיש להם שם משפחה זהה, מדובר על תאומים זהים עם גאווה כפולה במיוחד לאור העובדה שמאמרם פורסם לראשונה החודש במגזין המדעי והיוקרתי The Journal of Chemical Physics. המאמר נכתב בהנחייתה של ד"ר גילי ביסקר, בנושא: "Nonequilibrium self-assembly of multiple stored targets in a dimer-based system"
ד"ר ביסקר מפתחת במעבדה שלה ננו-חיישנים אופטיים תוך שימוש בתכונות האופטיות של ננו-צינוריות מפחמן כדי לזהות ולכמת מולקולות ביולוגיות בצורה ספציפית וסלקטיבית. בנוסף, היא חוקרת מערכות מורכבות מחוץ לשיווי משקל תרמודינמי, בהשראת מערכות ביולוגיות.
מערכות הרכבה עצמית
במערכות רבות, ובפרט בגוף האדם, מתרחשים תהליכים של הרכבה עצמית – תהליכים בהם מספר אבני בניין, כמו חלבונים, מסתדרים במבנה מסוים שנחוץ לפעולה ביולוגית ספציפית. כאשר תהליכי הרכבה עצמית מתרחשים בשיווי משקל תרמודינמי, כאשר חום נכנס מהסביבה או יוצא אליה רק באופן איטי ומבוקר, ניתן לתאר אותם ולחזות את תוצאותיהם מתוך התורה של מכניקה סטטיסטית בשיווי משקל.
אולם, תהליכים בגוף האדם מתאפיינים בחוסר שיווי משקל ואינם הפיכים, מה שמצריך כלים מתקדמים יותר על מנת לנתח אותם. במחקר, מודלה מערכת כללית של אבני בניין משני סוגים שונים שיכולות לשחזר מספר מבני מטרה, בהשראת מערכות ביולוגיות.
באמצעות סימולציות מחשב של המערכת, בהן הדינמיקה הוצאה משיווי משקל על ידי כוח לוקאלי (מקומי) – שמשפיע על האינטראקציה בין אבני בניין שכנות, הצליחו החוקרים להדגים מספר תכונות מעניינות. למשל, התאפשרה הרכבה של מבני המטרה מתוך מבנים התחלתיים קטנים יותר ביחס לאלו הנחוצים בשיווי משקל, הוגדלו מספר מבני המטרה שניתן לקודד למערכת, וכן שופרו היציבות ומהירות ההרכבה.
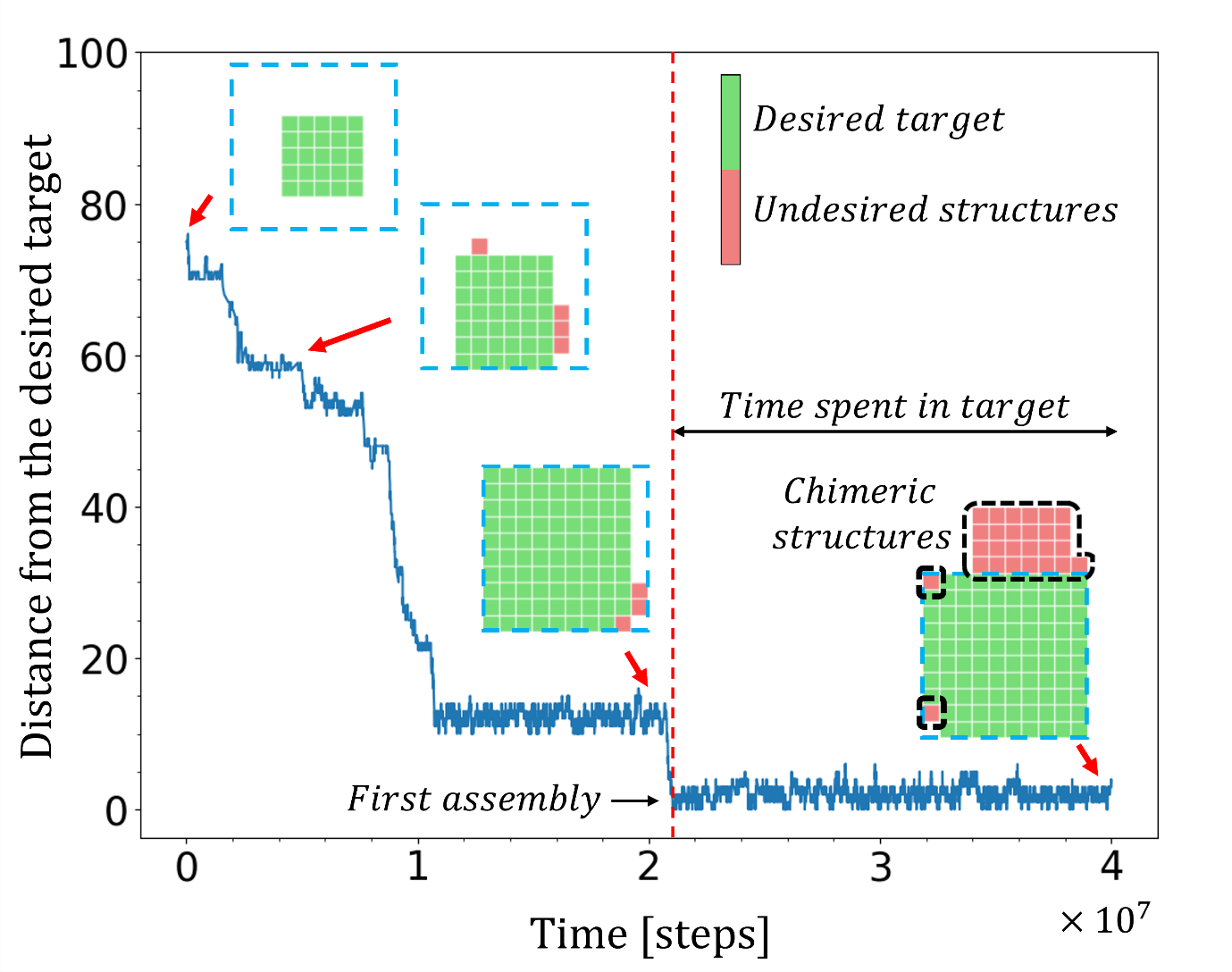
איור מתוך המאמר: סימולציה של הדינמיקה של המערכת. ככל שהזמן עובר, מצטרפים עוד חלקיקים לגרעין ההתחלתי ומבנה המטרה מורכב. בנוסף לחלק שחופף למבנה המטרה (בירוק), נבנים גם מבנים שגויים, שאינם שייכים למבנה המטרה (באדום).
איך המחקר יכול לסייע בעתיד?
מחקר זה יוכל לסייע בתכנון ושיפור מערכות המסוגלות לאחסן מספר מבני מטרה ולשחזר אותם, למשל חומרים מסתגלים שיכולים להסתדר במבנים שונים כתלות בתנאים חיצוניים. בפרט, הקטנת המבנים ההתחלתיים הדרושים, כפי שהוצג במחקר, יכולה להוות בסיס לאחסון יעיל יותר של מידע באמצעות מערכות מורכבות.
אלה שמתאהבים בבעיה הם אלה שממציאים לה פתרון

מחקר
לראשונה, חוקרות מהנדסה ביו-רפואית הצליחו בעזרת ננו-צינוריות מפחמן לבצע מעקב בתוך תולעים מבלי שתהיה הפרעה של אוטופלורנסציה מהתולעת עצמה

מולקולות או חלקיקים פלורסנטים, הפולטים אור באורך גל מסויים בעקבות עירורם באור בעל אורך גל קצר יותר, מהווים כלי נפוץ במחקרים רבים. לרוב, חוקרים משתמשים בצבענים פלורסנטים על מנת לסמן ולעקוב אחר חלבונים או מטרות ברקמות שונות בתוך חיות מודל. במקרה של תולעים, הסימון לא פשוט בכלל, היות ולתולעת עצמה יש חלבונים שפולטים פלורסנציה בתחום האור הנראה באורכי גל זהים לאורכי הגל בהם פולטים הצבענים הפלורסנטיים.
בעזרת פיתוח חדש, המבוסס על ננו צינוריות מפחמן של ד"ר ביסקר, הודגמה יכולת דימות ומעקב בתוך התולעים מבלי שתהיה הפרעה של אוטופלורנסציה מהתולעת עצמה, בזכות הפליטה הפלורסנטית של ננו-הצינוריות בתחום האינפרא-אדום הקרוב.
עבודתה של ד"ר גילי ביסקר ומנהלת המעבדה שלה ד״ר עדי הנדלר-נוימרק בנושא, התפרסמה בכתב העת המדעי Materials Today Bio בה הן חושפת את השיטה החדשנית למעקב אחר ננו-הצינוריות מפחמן בתוך תולעים. במחקר הייתה שותפה גם ד״ר ורנה וולף, פוסטדוקטורנטית במעבדתה של גילי.
ד"ר ביסקר מפתחת במעבדה שלה ננו-חיישנים אופטיים תוך שימוש בתכונות האופטיות של ננו-הצינוריות מפחמן כדי לזהות ולכמת מולקולות מטרה בצורה ספציפית וסלקטיבית. החיישנים מבוססים על ננו-צינוריות מפחמן הפולטות פלורסנציה בתחום האינפרא-אדום הקרוב, וכך מתאפשר לראות עמוק יותר בתוך הרקמה ובדוגמאות ביולוגיות, ולשפר את היחס בין האות לרעש.
תולעים כחיית מודל
תולעים משמשות חיית מודל נפוצה בזכות דמיון גנטי גבוה לבני אדם בגנים מחוללי מחלות כמו למשל במחלת הפרקינסון. למרות היתרונות הרבים שלהן כגון גודלן הקטן ושקיפותן, חסרון אחד משמעותי הוא האוטופלורסנציה שלהן בכל התחום הנראה, הנובעת מחלבונים שנמצאים בתוך התולעת עצמה הפולטים פלורסנציה. חסרון זה קיים לא רק בתולעים, אלא בחיות מודל רבות, עובדה המקשה מאוד על שימוש בצבענים או חלבונים פלורסנטים סינתטיים, היות ולא ניתן להפריד בין החלבונים הפלורסנטים הטבעיים של האורגניזמים לבין הצבען הפלורסנטי הסינתטי.
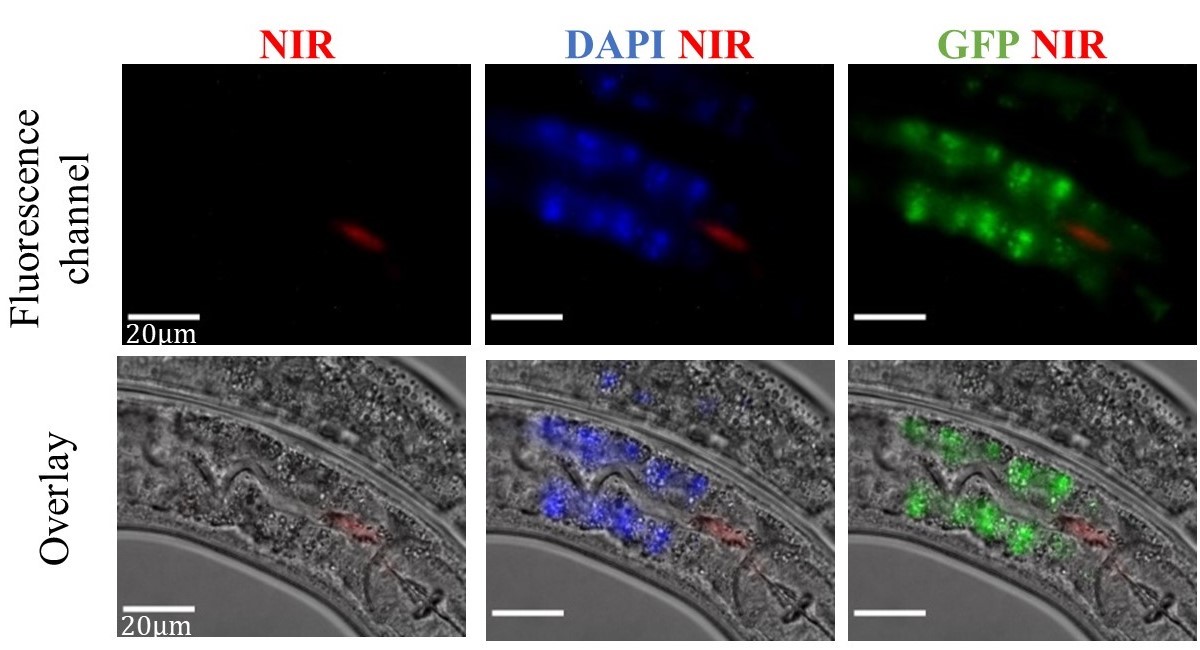
תמונה מהמאמר: בשורה העליונה ניתן לראות תמונות פלורסנטיות של התולעים במספר אורכי גל, התמונה השמאלית (NIR) היא של ננו-הצינוריות (אדום). התמונה האמצעית (DAPI+NIR) והימנית (GFP+NIR) הן תמונות משולבות של ננו-הצינוריות מפחמן באדום עם התמונות של האוטופלורסנציה של התולעת באורך גל המתאים לצבע הפלורסנטי הסינתטי DAPI או GFP (כחול או ירוק). בשורה השנייה התמונות הפלורסנטיות מוצגות על גבי תמונה באור לבן של התולעים, על מנת למקם את ננו-הצינוריות ביחס למעי של התולעת.
החוקרות השתמשו בננו-צינוריות מפחמן אשר פולטות פלורסנציה בתחום האינפרא אדום הקרוב – זהו תחום ספקטרלי בו אין אוטופלורסנציה כלל. "באמצעות ננו-הצינוריות הצלחנו לעקוב אחר פעילות העיכול של התולעים, לראות את המעבר שלהן בוושט עד צינור המעי, ולנטר את פעילות השאיבה של האוכל", מסבירה ד"ר הנדלר-נוימרק.
לדברי ד״ר ביסקר, ״הננו-חלקיקים הללו מתאימים לעבודה עם דוגמאות ביולוגיות ואינם פוגעים בהן, ולכן מאפשרים לעקוב אחר תהליכים בתוך אורגניזמים או תאים חיים ללא הפרעה של האוטופלורנסנציה הטבעית שלהם. השימוש בננו-צינוריות מפחמן יכול להוות יתרון משמעותי במעקב אחר תהליכים בחיות מודל קטנות כמו תולעים וגם לעקוף לחלוטין את האתגר של אוטופלורסנציה בתחום האור הנראה״.
אלה שמתאהבות בבעיה הן אלה שממציאות לה פתרון
מחקר
המחקר נערך בשיתוף חוקרים מהנדסה ביו-רפואית, בית הספר סגול למדעי המוח, מדעי המחשב והאוניברסיטה העברית

כמעט שנתיים אחרי שהפכה למגפה עולמית, שקטלה מיליוני בני אדם, עדיין לא נפתרה התעלומה אילו חלבונים בנגיף ה-SARA-CoV-19 אחראים לנזק החמור לכלי הדם שעשוי אף להוביל להתקף לב או לשבץ. כעת, צוות מומחים בהובלת אוניברסיטת תל אביב הצליח לזהות לראשונה חמישה חלבונים מבין 29 החלבונים המרכיבים את הנגיף שאחראים לפגיעה בכלי הדם. החוקרים מקווים כי זיהוי החלבונים יסייע בפיתוח תרופות ייעודיות לקורונה ויביא להפחתת הפגיעה בכלי הדם.
המחקר נערך בהובלת קבוצות המחקר של ד"ר בן מעוז מהמחלקה להנדסה ביו-רפואית ובית הספר סגול למדעי המוח, פרופ' אורי אשרי מבית הספר סגול למדעי המוח והפקולטה למדעי החיים, ופרופ' רודד שרן מבית הספר למדעי המחשב ע"ש בלווטניק - כולם חוקרים באוניברסיטת תל אביב. במחקר השתתפו גם פרופ' יעקב נחמיאס מהמכון למדעי החיים באוניברסיטה העברית, והחוקרים ד״ר רוסאנה ראוטי, ד״ר יעל ברדוגו והדוקטורנט מיישר שחוח מאוניברסיטת תל אביב. תוצאות המחקר החדש התפרסמו בכתב העת eLife.
"אנחנו רואים שכיחות גבוהה מאוד של מחלות כלי דם וקרישת דם, דוגמת שבץ והתקף לב, בקרב חולי קורונה", מסביר ד"ר בן מעוז. "אנחנו רגילים לחשוב על קורונה כעל מחלה נשימתית בעיקרה, אבל האמת היא שחולי קורונה נמצאים בסיכון מוגבר עד פי שלושה לעבור שבץ או התקף לב למשל. כל העדויות מראות שהנגיף פוגע קשות בכלי הדם או בתאי האנדותל העוטפים את כלי הדם. אלא שעד היום התייחסו לנגיף כולו כאל מקשה אחת. אנחנו רצינו לגלות אילו חלבונים בתוך הנגיף אחראים לנזק הזה".
נגיף הקורונה החדש הוא נגיף פשוט יחסית – והוא מורכב בסך הכול מ-29 חלבונים שונים (לעומת עשרות אלפי חלבונים שמייצר גוף האדם). החוקרים מאוניברסיטת תל אביב השתמשו ב-RNA של כל אחד מחלבוני הקורונה ובדקו את התגובה שנוצרת כאשר מחדירים את רצפי ה-RNA השונים לתאים אנושיים של כלי דם במעבדה, וכך הצליחו לזהות חמישה חלבוני קורונה שפוגעים בכלי הדם.
"כשנגיף הקורונה חודר לגוף, הוא מתחיל לייצר 29 חלבונים, נוצר נגיף חדש, הוא מייצר 29 חלבונים חדשים וכך הלאה", מספר ד"ר מעוז. "בתהליך הזה, כלי הדם שלנו הופכים מצינורות אטומים למעין רשתות או חתיכות בד חדירות, ובמקביל חלה הגברה בקרישת הדם. אנחנו בדקנו ביסודיות את ההשפעה של כל אחד מ-29 החלבונים שהנגיף מבטא, והצלחנו לראשונה לזהות חמישה חלבונים ספציפיים שמחוללים את הנזק הגדול ביותר לתאי האנדותל ומכאן גם ליציבות ולתפקוד כלי הדם. בנוסף, השתמשנו במודל חישובי שפותח על ידי פרופ' שרן, המאפשר לשער ולזהות אילו מחלבוני הקורונה הם בעלי ההשפעה הגדולה ביותר על רקמות נוספות פרק לכלי הדם, וזאת מבלי שראינו אותם ב'פעולה' במעבדה".
לדברי ד"ר מעוז, לזיהוי החלבונים עשויות להיות השלכות משמעותיות במאבק במחלה. "המחקר שלנו יכול לסייע במציאת מטרות לתרופה שתשמש לעצירת פעילותו של הנגיף, או לפחות למזעור הנזק בכלי הדם".

מחקר
החוקרים, בהובלת פרופ' תמיר טולר וסטודנטית המחקר טל גוטמן הצליחו לנבא את סוג הסרטן ואת שיעור התמותה ממנו לפי מוטציות "שקטות" בגנומים הסרטניים – הוכחת היתכנות שיכולה בעתיד להציל חיי

מוטציות "שקטות" מוגדרות ככאלה שלא משנות את רצף חומצות האמינו של החלבונים. בשנים האחרונות מצטברות הראיות לכך שמוטציות שקטות, הן בתוך והן מחוץ לאזור הקידוד הגנטי בתא, יכולות להשפיע על ביטוי גנים וכי ייתכן שהן קשורות להתפתחות ולהתפשטות של תאים סרטניים. עם זאת, עד כה לא נבדק כמותית האם המוטציות הללו יכולות לתרום לזיהוי סוג הסרטן ולניבוי סיכויי השרידות של החולה.
במחקר החדש, המבוסס על כשלושה מיליון מוטציות מגנומים סרטניים של 9,915 חולים, החוקרים ניסוי לבדוק האם הם יכולים לזהות את סוג הסרטן ולהעריך את שיעור התמותה ממנו 10 שנים לאחר האבחנה הראשונית אך ורק על סמך המוטציות השקטות – ומצאו כי יכולת הפרדיקציה של המוטציות השקטות דומה בהרבה מיקרים לביצועי הפרדיקציה המקובלת של המוטציות ה"רגילות". בנוסף ניסו החוקרים להעריך האם שילוב של מידע על מוטציות שקטות ורגילות יכולות לשפר יכולת הסיווג של סוג הסרטן, ומצאו כי המידע שמתקבל ממוטציות שקטות משפר את מרווח הטעות ב-68%. בסוגים מסוימים של סרטן מדובר בשיפור של עד 17% ביכולת הסיווג, כאשר שילוב שני סוגי המוטציה יכול לשפר את הפרוגנוזה בשיעור של עד 5%.
"בגנום שלנו, כמו בכל גנום של כל יצור חי אחר, ישנן מוטציות שיכולות לשנות את רצף חומצות האמינו של החלבונים שמקודדים בגנום", מסביר פרופ' טולר. "מאחר שהחלבונים הללו אחראים על המנגנונים השונים בתא, מוטציות כאלה מעורבות בהפיכת התא הבריא לתא סרטני. לעומתן, יש מוטציות שלא משנות את חומצות האמינו, ולכן קראו להן 'שקטות' והתעלמו מהן במשך שנים רבות. אנחנו ערכנו בפעם הראשונה אנליזות לכ-10,000 גנומים סרטניים מכל הסוגים, והראינו שיש למוטציות השקטות ערך דיאגנוסטי, איזה סוג סרטן זה, וגם ערך פרוגנוסטי, כמה זמן החולה ישרוד".
לדברי פרופ' טולר, החומר הגנטי בתא מחזיק בשני סוגים של מידע: מה רצף חומצות האמינו שמיוצר – ומתי וכמה לייצר מכל חלבון – כלומר הרגולציה של תהליך הייצור. "אותן מוטציות שקטות יכולות להשפיע על הרגולציה של ביטוי גנים, וזאת השפעה לא פחות חשובה מסוג החלבון שמיוצר. מן הסתם אם התא מייצר הרבה פחות מחלבון מסוים – זה גרוע כמעט כמו למחוק אותו. השפעה נוספת היא קיפול החלבון. החלבון הוא מולקולה ארוכה שכוללת בדרך כלל מאות רבות של חומצות אמינו, כאשר הקיפול התלת ממדי של המולקולה מתחיל כבר כשהן מיוצרות בריבוזום. קצב הייצור של החלבון על ידי הריבוזום משפיע על הקיפול, והמוטציות השקטות יכולות להשפיע על קצב הייצור של החלבון ולכן על הקיפול שלו – קיפול שהוא משמעותי לתפקוד בפועל. בנוסף, יש מקרים בהם המוטציות השקטות משפיעות על תהליך בשם שיחבור, שבו חתיכות מהחומר הגנטי נחתכות ליצירת הרצף הסופי שממנו ייווצר החלבון. בקיצור, מסתבר שהמוטציות השקטות האלה עושות הרבה מאוד רעש, ואנחנו הצלחנו לראשונה לכמת את ההשפעה שלהן".
כדי לבחון את השערתם ולכמת את השפעת המוטציות הללו, פרופ' טולר ועמיתיו השתמשו במידע גנטי ציבורי על גנומים סרטניים מהמכונים הלאומיים לבריאות (NIH) בארה"ב. החוקרים לקחו הנתונים על הגנום הסרטני וניסו בשיטות המבוססות על למידת מכונה לנבא מה סוג הסרטן וכמה שנים חי כל חולה לפי המוטציות השקטות – ולאחר מכן השוו את התוצאות שקיבלו לנתוני האמת מהמאגר.
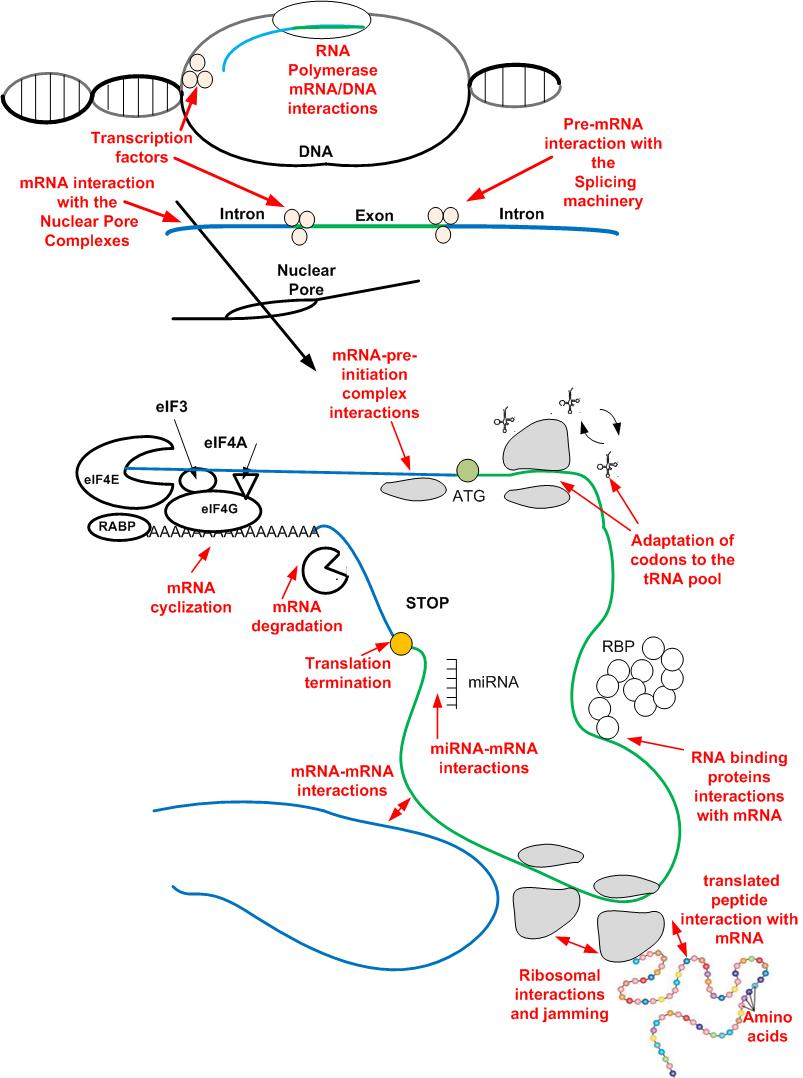
תמונה: אילוסטרציה של אינטראקציות שונות של החומר הגנטי עם פקטורים בתא שמבקרים את רמות הביטוי. מוטציות שקטות יכולות להשפיע על יעילות האינטראקציה עם הפקטורים האלה בתא הסרטני, ולכן להשפיע על רמות הביטוי של גנים שמשפיעים על השרידות של התא הסרטני.
"לתוצאות המחקר מספר השלכות חשובות", אומר פרופ' טולר. "קודם כל שימוש במוטציות שקטות בהחלט יכול לשפר מודלים שחוזים פרוגנוזה ומשמשים לסיווג. חשוב לציין שגם לשיפור של 17% יש משמעות גדולה מאוד כי מאחורי המספרים האלה עומדים בני אדם שאנחנו אוהבים, ויום אחד אולי אנחנו עצמנו, לכן כל שיפור של אחוז הוא דרמטי. רופא שמגלה גרורות רוצה לדעת מה מקור הגרורה ומה מסלול התפתחות המחלה, כדי להתאים את הטיפול הטוב ביותר. אם למשל במקום דיאגנוסטיקה ופרוגנוסטיקה שגויות לחמישה מבין עשרה חולי סרטן נגיע למצב שבו שוגים רק בארבעה מכל עשרה חולי סרטן, זה יכול להיתרגם בסופו של דבר למיליוני חולים שאולי ניתן להציל את חייהם. בנוסף, התוצאות שלנו מראות שרק על סמך מוטציות שקטות ניתן במקרים רבים לקבל ביצועי ניבוי דומים להסתמכות על מוטציות שהן לא שקטות. זו תוצאות מעודדת, מכיוון שבשנים האחרונות מפותחות טכנולוגיות שמסווגות סרטן על סמך בדיקות דם לא פולשניות יחסית, המבוססות על אנליזה של חתיכות דנ"א ממקור סרטני. מאחר שרוב הדנ"א שלנו לא מקודד לחלבון, סביר להניח שרוב החתיכות מסוג זה שנדוג יכילו מוטציות שקטות".
למחקר החדש השלכות לכלל תחומי המחקר והטיפול האונקולוגי, ואחרי הוכחת ההיתכנות הזאת בכוונת החוקרים להקים סטארטאפ עם חממת "סאנרה", שיתמקד במוטציות השקטות ככלי רפואי לכל דבר ועניין.
עוד השתתפו במחקר: גיא גורן ועומרי עפרוני
למאמר ב npj genomic medicine
אלה שמתאהבים בבעיה הם אלה שממציאים לה את הפתרון

מחקר
סטודנטית לתואר שני וחוקרת מהפקולטה להנדסה פיתחו פלטפורמה שבעתיד תוכל לאפשר ניטור ספיחת אינסולין ברקמה לאחר הזרקה על ידי משאבת אינסולין, ובכך לשפר את הטיפול הניתן לחולי סוכרת.

רוני ארליך היא סטודנטית לתואר שני בהנדסה ביו-רפואית במעבדה של ד"ר גילי ביסקר "המעבדה לאופטיקה, ננו-סנסורים, וביופיזיקה" שמפתחת וחוקרת יחד עם חברי המעבדה ננו-חיישנים אופטיים. לאחרונה מאמרה בהנחיית ד"ר ביסקר התפרסם במגזין המדעי Small, ואף נבחר להופיע על הכריכה של הגיליון הקרוב של Small שיצא לאור ב 28 ליולי. במחקר השתתפו גם ד״ר עדי הנדלר-נוימרק ד״ר ורנה וולף ודין אמיר
המאמר של רוני עוסק בפיתוח פלטפורמה חדשנית היכולה לספק משוב מידי על הפרשת אינסולין מתאי בטא באמצעות סיגנל אופטי. תאי הבטא, הם התאים בלבלב האחראים על ייצור והפרשת אינסולין על מנת לווסת את רמות הסוכר בדם.
המעבדה של ד"ר ביסקר מתמקדת בפיתוח כלים ננו-טכנולוגיים שיאפשרו לעקוב אחרי תהליכים מולקולריים, בשאיפה להבין את הדינמיקה של אותם תהליכים. כלים אלו מבוססים על ננו-חלקיקים הפולטים פלורסנציה בתחום האינפרא-אדום, ויכולים לגלות שינויים בסביבה הקרובה שלהם או ספיחה של מולקולות על פני השטח שלהם. בעזרת מעקב אחרי התכונות האופטיות של הננו-חלקיקים הללו במערכות ביולוגיות אפשר ללמוד עליהן ולקבל מידע חדש על תהליכים מיקרוסקופיים שאחראיים על ההתנהגות המקרוסקופית שלהן.
תגליות במאמר שפורסם
המחקר כלל את פיתוח הסנסורים לאינסולין, אפיונם, והדגמה של השימוש בהם. הסנסורים מבוססים על ננו-צינוריות מפחמן שעברו אקטיבציה המאפשרת זיהוי בזמן אמת של מולקולת המטרה. ננו-הצינוריות מפחמן פולטות פלורסנציה בתחום האינפרא-אדום הקרוב, ובכך מאפשרים דימות בעומק רקמות ודוגמאות ביולוגיות. עוצמת האות הפלורסנטי של החיישנים משתנה עקב קישור האינסולין לפני השטח של הננו-צינוריות וכך מתקבל המשוב על זיהוי מולקולות האינסולין.
באמצעות עקומת כיול עבור ריכוזים שונים של אינסולין ניתן להסיק ריכוז לא ידוע של אינסולין מתוך התגובה הפלורסנטית. "במחקר זה הדגמנו בפעם הראשונה את השימוש בננו-צינוריות הפחמן לזיהוי אינסולין בתרבית תאי בטא המפרישים אינסולין בתגובה לגלוקוז. מתוך אנליזה של התגובה הפלורסנטית הצלחנו לכמת באופן מדויק את כמות האינסולין שמופרש ע"י תאי הבטא ולקבל משוב בזמן אמת על יכולת התפקוד של התאים" מסבירה רוני.
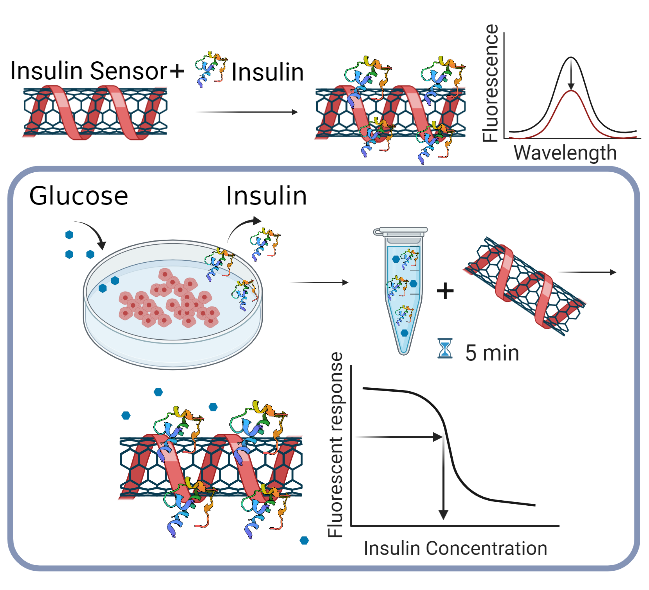
בתמונה: איקטוב הננו-צינוריות בצורה חכמה הפך אותן לסנסורים אופטיים לאינסולין. בתגובה לקישור של האינסולין לסנסורים, עוצמת האות הפלורסנטי של הננו-צינוריות משתנה וכך מתקבל המשוב על זיהוי מולקולות האינסולין. מתוך התגובה הפלורסנטית ניתן לחשב באופן מדויק את כמות האינסולין המופרש מתאי הבטא.
בשורה משמחת לחולי הסוכרת
פיתוח זה יכול לתרום למחקר בתחום מנגנוני מחלת הסוכרת הקשורה בתפקוד לא תקין של תאי הבטא, בעזרת היכולת לקבל משוב בזמן אמת על פעילותם. בעתיד, הסנסורים יוכלו לאפשר ניטור ספיחת אינסולין ברקמה לאחר הזרקה על ידי משאבת אינסולין, ובכך לשפר את הטיפול הניתן לחולי סוכרת.
האישה מאחורי המחקר
רוני סיימה את התואר הראשון שלה במחלקה להנדסה ביו-רפואית ב- 2019 ומיד המשיכה לתואר שני בקבוצה של ד״ר גילי ביסקר. במהלך התואר השני זכתה במלגת משרד המדע ללימודי תואר שני בהנדסה ובמדעים מדוייקים, במלגת הצטיינות של מכון גרטנר למערכות רפואיות ננומטריות, ובמלגת הצטיינות לתואר שני של הפקולטה להנדסה באוניברסיטת תל אביב. רוני נשואה לאריאל מ"פ לוחם בחיל בשריון ובמהלך התואר הראשון נולדו לה שתי בנות מקסימות עלמא (4) ומאיה (2) – כבר אמרנו superwoman אמיתית?
הקליקו למאמר המלא כאן.
אלה שמתאהבים בבעיה הם אלה שממציאים לה פתרון

מחקר
חוקרים מהפקולטה להנדסה ואוניברסיטת תל אביב יצרו חיישן שניתן להשתיל אותו בכל מקום בגוף, החיישן מתחבר לעצב אחר שמתפקד בצורה תקינה ומחזיר לעצב הפגוע חלק מתחושת המגע.

טכנולוגיה חדשה ופורצת דרך של אוניברסיטת תל אביב מעוררת תקווה בקרב אנשים שאיבדו את תחושת המגע בעצבים של איברים שונים בעקבות קטיעה או פציעה. הטכנולוגיה שנוסתה על חיות מודל בהצלחה רבה כוללת חיישן זעיר שמושתל בעצב של האיבר הפגוע, למשל באצבע, והוא מחובר ישירות לעצב תקין ובכל פעם שהאיבר נוגע בחפץ אחר, החיישן מופעל ומעביר זרם חשמלי לעצב הבריא, פעולה אשר משחזרת את תחושת המגע. החוקרים מדגישים כי מדובר בטכנולוגיה "בריאה" שמותאמת לגוף האדם וניתן להשתיל אותה בכל מקום בגוף.
הטכנולוגיה פותחה בהובלת צוות מומחים מאוניברסיטת תל אביב: ד"ר בן מעוז, יפתח שלומי, שי דיולד וד"ר יעל ליכטמן-ברדוגו מהמחלקה להנדסה ביו-רפואית ובשיתוף קשת תדמור מבית הספר סגול למדעי המוח וד"ר עמיר ערמי מהפקולטה לרפואה ע"ש סאקלר ומהיחידה למיקרוכירורגיה במחלקה לכירורגיה של היד, המרכז הרפואי שיבא. המחקר התפרסם בכתב העת היוקרתי ACS NANO.
החוקרים מספרים כי הפרויקט הייחודי התחיל בפגישה בין שני חברים מאוניברסיטת תל אביב: ד"ר עמיר ערמי מהפקולטה לרפואה ומיחידת המיקרו-כירורגיה בשיבא וד"ר בן מעוז מהמחלקה להנדסה ביו-רפואית ובית ספר סגול למדעי המוח. "דיברנו על האתגרים בעבודות שלנו", מספר ד"ר מעוז, "וד"ר ערמי שיתף אותי בקושי שהוא חווה בטיפול באנשים שמאבדים את יכולת החישה באיבר זה או אחר כתוצאה מפציעה. צריך להבין שמדובר בקשת רחבה מאוד של פציעות, החל מפציעות קלות – לדוגמה, מישהו חותך סלט ונחתך מהסכין – ועד לפציעות קשות מאוד. גם אם ניתן לאחות את הפצע ולתפור את העצב הפגוע, במקרים רבים התחושה נותרת פגועה. החלטנו להתמודד יחד עם האתגר הזה, ולמצוא פתרון שיחזיר לפגועים את יכולת החישה".
יובהר כי בשנים האחרונות תחום הנוירו-תותבים מבטיח לשפר את חייהם של אלה שאיבדו את התחושה על ידי השתלת חיישנים במקום העצבים הפגועים. אלא שלטכנולוגיה הקיימת מספר חסרונות משמעותיים, כמו ייצור ושימוש מורכבים וכן צורך במקור כוח חיצוני כמו סוללה. כעת, חוקרים מאוניברסיטת תל אביב השתמשו בטכנולוגיה חדישה בשם ננו-גנרטור טריבו-אלקטרי (Nanogenerator triboelectric, או TENG) כדי להנדס ולבדוק על חיות מודל חיישן זעיר שמחזיר את התחושה באמצעות זרם חשמלי שמגיע ישירות מעצב בריא וללא צורך בהשתלה מורכבת או בהטענה.

במסגרת הפיתוח הטכנולוגי החוקרים יצרו חיישן שניתן להשתיל אותו על עצב פגום מתחת לקצה של האצבע, והוא מחזיר למושתל חלק מיכולת החישה באצבע. הפיתוח הייחודי אינו מצריך שימוש במקור מתח חיצוני כגון חשמל או סוללות. החוקרים מסבירים כי החיישן פועל למעשה על כוח החיכוך: בכל פעם שהמכשיר מרגיש חיכוך, הוא נטען לבד.
מדובר בשני לוחות זעירים בגודל של פחות מחצי ס"מ על חצי ס"מ. כשהלוחות האלה באים במגע אחד עם השני, הם משחררים מטען חשמלי שמועבר לעצב הבריא. באופן הזה, כשהאצבע הפגועה נוגעת במשהו, הנגיעה משחררת מתח בהתאם ללחץ שהופעל על המכשיר – מתח חלש למגע חלש ומתח חזק למגע חזק – ממש כמו חישה רגילה.
לטענת החוקרים ניתן להשתיל את המכשיר בכל מקום בגוף בו יש צורך בשחזור תחושה למגע, והוא עוקף למעשה את אברי החישה הפגועים. כמו כן, החומר שממנו עשוי המכשיר הוא ידידותי לגוף האדם, הוא לא דורש תחזוקה, ההשתלה פשוטה והמכשיר עצמו אינו נראה מבחוץ.
לדבריו של ד"ר מעוז, לאחר שבדקו את החיישן החדש במעבדה (יותר מחצי מיליון הקשות אצבע עם המכשיר), החוקרים השתילו אותו בכפות רגליהם של חיות מודל. החיות הלכו כרגיל, מבלי לחוות כל פגיעה בעצבים המוטוריים, ובבדיקות הוכח כי החיישן אפשר להן להגיב לגירויים סנסוריים. "בדקנו את הפיתוח שלנו על חיות מודל, והתוצאות היו מעודדות מאוד", מסכם ד"ר מעוז. "בשלב הבא נרצה לבחון את המשתל על מודלים גדולים יותר ובהמשך – להשתיל את החיישנים שלנו גם באצבעותיהם של בני אדם שאיבדו את יכולת החישה. היכולת הזו עשויה לשפר באופן משמעותי את התפקוד ואת איכות החיים, וחשוב מכך: להגן עלינו מפני סכנה. אנשים שלא יכולים להרגיש מגע גם לא יכולים להרגיש שהאצבע שלהם נמחצת, נשרפת או קופאת".
מחקר
ד"ר בן מעוז מהנדסה ביו-רפואית בשיתוף חוקרים ומומחים מאוניברסיטת תל אביב חיברו אוזן אמיתית של חגב – לרובוט

פיתוח טכנולוגי וביולוגי של אוניברסיטת תל אביב, חסר תקדים בארץ ובעולם, מאפשר לראשונה לחבר אוזן של בעל חיים מת (חגב) לרובוט שקולט את האותות החשמליים של האוזן ומגיב בהתאם. התוצאה מיוחדת במינה: החוקרים מוחאים מחיאת כף אחת, האוזן של החגב שומעת את הצליל והרובוט נוסע קדימה. החוקרים מוחאים שתי מחיאות כף, האוזן שומעת – והרובוט נוסע אחורה".
המחקר האינטרדיסציפלינרי נערך בהובלת ד"ר בן מעוז מהמחלקה להנדסה ביו-רפואית ובית הספר סגול למדעי המוח, בשיתוף צוות מומחים מבית הספר לזואולוגיה ובית הספר סגול למדעי המוח: פרופ' יוסי יובל, פרופ' אמיר אילי, ד"ר אנטון שיינין, עידן פישל, יוני עמית, נטע שביל. תוצאות המחקר התפרסמו בכתב העת היוקרתי Sensors.
החוקרים מסבירים שבתחילת המחקר הם ביקשו לבחון כיצד ניתן לשלב את היתרונות של המערכות הביולוגיות גם במערכות הטכנולוגיות, ואיך אפשר להשתמש בחושים של בעלי חיים מתים כחיישנים לרובוט. "בחרנו בחוש השמיעה, כי אפשר להשוות אותו בקלות לטכנולוגיות קיימות – בניגוד לריח למשל ששם האתגר גדול עוד יותר", מדגיש ד"ר מעוז. "האתגר שלנו היה להחליף את המיקרופון אלקטרוני של הרובוט באוזן של חרק מת, לנצל את היכולת של האוזן לקלוט את האותות החשמליים מהסביבה, במקרה הזה את הוויברציות באוויר, ובאמצעות שבב מיוחד להמיר את קלט החרק לקלט של רובוט".
לצורך המשימה הייחודית והלא שגרתית, בשלב הראשון החוקרים במעבדה של ד"ר מעוז בנו רובוט שמסוגל להגיב לאותות שהוא מקבל מהסביבה. לאחר מכן, בשיתוף פעולה רב תחומי החוקרים הצליחו לבודד ולאפיין את האוזן של חגב מת, להצליח להחזיק אותה בחיים, כלומר מתפקדת, מספיק זמן כדי ניתן לחבר אותה בהצלחה לרובוט. בשלב האחרון החוקרים הצליחו למצוא דרך לקלוט את האותות שנקלטים באוזן החגב בדרך שתהיה שימושית גם לרובוט. בסוף התהליך, הרובוט הצליח 'לשמוע' את הצלילים ולהגיב בהתאם.

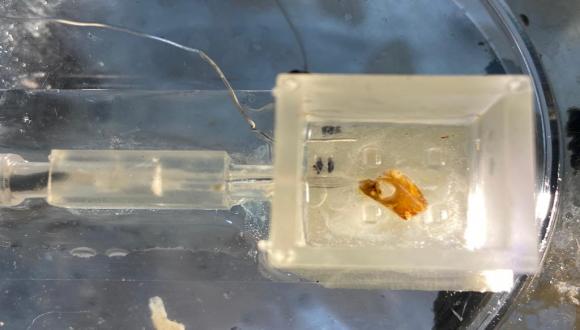
בתמונה: הרובוט עם הצ'יפ
"מעבדתו של פרופ' אילי בעלת ניסיון רב בעבודה עם חגבים, והם פיתחו מיומנויות לבודד את האוזן ולאפיין אותה", מסביר ד"ר מעוז. "מעבדתו של פרופ' יובל בנתה את הרובוט ופיתחה קוד המאפשר לרובוט להגיב לאותות חשמליים של קול. ואילו המעבדה שלי פיתחה מכשיר מיוחד – אוזן-על-שבב – שמאפשר לשמור את האוזן חיה זמן לאורך הניסוי באמצעות אספקה של חמצן ומזון לאיבר, ובמקביל מאפשר להוציא את הסיגנלים החשמליים מאוזן החגב, להגביר ולהעביר אותם לרובוט".
ככלל, למערכות ביולוגיות יתרון עצום על מערכות טכנולוגיות – הן מבחינת הרגישות והן מבחינת תצרוכת האנרגיה. לכן הפרויקט של חוקרי אוניברסיטת תל אביב פותח פתח לשילובים חושיים בין רובוטים לחרקים – ועשוי לייתר פיתוחים מסורבלים ויקרים בהרבה בתחום הרובוטיקה.
"צריך להבין שמערכות ביולוגיות מוציאות אנרגיה זניחה ביחס למערכות אלקטרוניות. הן ממוזערות, ולכן גם חסכוניות ויעילות, בצורה קיצונית. לשם השוואה, מחשב נייד צורך כ-100 וואט לשעה, ואילו המוח האנושי צורך כ-20 וואט ביממה. הטבע מתקדם מאיתנו בהרבה, לכן כדאי להשתמש בו. ניתן להשתמש בעיקרון שהצגנו, וליישם אותו על חושים אחרים, כמו ריח, ראייה ומישוש. לדוגמה, לבעלי חיים מסוימים יש יכולות מדהימות לזיהוי של חומרי נפץ וסמים, וייצור של רובוט עם אף ביולוגי יוכל לעזור לנו לשמור על חיי אדם ולזהות עבריינים באופן שלא ניתן כיום. יש בעלי חיים שיודעים לזהות מחלות ואחרים שיודעים לחוש רעידות אדמה. השמיים הם הגבול".
אלה שמתאהבים בבעיה הם אלה שממציאים לה פתרון
מחקר
מאמרו של פרופ' עמית גפן פורסם לאחרונה בכתב עת יוקרתי בנושא טיפול בלחץ שלילי בפצע באמצעות וואקום

פרופ' עמית גפן, ראש המעבדה לביו-מכניקה של מערכת השלד והשרירים במחלקה להנדסה ביו-רפואית באוניברסיטת תל אביב ומומחה עולמי במניעה וטיפול בפצעי לחץ, פרסם מאמר חדש בכתב העת .Medical Engineering & Physics
פצעי לחץ
פצעי לחץ הינם אחת הבעיות החמורות ביותר איתן מתמודדות מערכות בריאות בעולם כולו, הן מבחינת סבל לחולים ולמשפחות והן מבחינת עלות הטיפול. הפצעים הללו הם גם גורם תמותה משמעותי ומובן שיש לעשות הכל כדי למנוע אותם. מחקריו של פרופ' גפן מתמקדים בהבנת אופן התפתחות פצעי לחץ וכן כיבים סוכרתיים בכל הרמות – מהאופן שבו מתים תאים בודדים בגוף ועד לנזק הנראה לעין. הבנות אלו מאפשרות למצוא דרכי מניעה וטיפול יעילות יותר כדי למנוע מוות וסבל של מיליונים רבים.
טיפול בלחץ שלילי
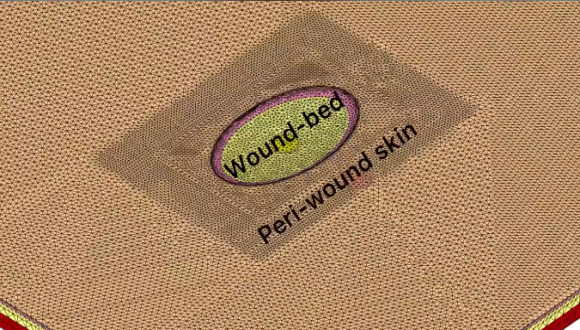
טיפול בפצעים באמצעות לחץ שלילי (וואקום) הוא פרקטיקה קלינית מקובלת לריפוי חתכים כתוצאה מניתוחים כירורגיים ופצעים כרוניים, הכוללת הפעלת לחץ שלילי באמצעות משאבה המחוברת לחבישת ספוג הממוקמת על גבי הפצע. עם זאת, ההשפעות הביומכניות של טיפול זה אינן מובנות עדיין ולכן פותח בקבוצת המחקר של פרופ' עמית גפן מודל חישובי מתקדם ביותר מסוגו לצורך סימולציות של עוצמת העומסים המכניים והתנאים הביומכניים המתפתחים ברקמות הפצע וסביבו.
המודל החישובי החדש מאפשר לחקור את השפעות גודל הלחץ השלילי ותכונות חבישת הספוג על התנאים הביומכניים השוררים ברקמות. המודל זיהה בהצלחה את הפרמטרים החשובים באמצעותם ניתן לשלוט על התנאים ברקמות סביב הפצע, שהם קריטיים לצורך ריפוי והחלמה.
המודל והתוצאות שהושגו באמצעותו דווחו לאחרונה בכתב-העת Medical Engineering & Physics. העבודה בוצעה במימון מענק מחקר STINTS של הקהילה האירופית בנושא בריאות ותפקוד העור ומענק משרד המדע והטכנולוגיה בנושא מכשירים רפואיים באינטראקציה עם העור שהוענקו לפרופ' עמית גפן - שהוא וקבוצת המחקר שלו מובילים עולמיים בנושאים הללו.
אלה שמתאהבים בבעיה הם אלה שממציאים לה פתרון
מחקר
עבודותו האחרונה של פרופ' עמית גפן פורסמה השבוע בכתב העת Journal of Wound Care בנושא COVID-19, מסכות פנים ונזקי עור

פרופ' עמית גפן מהמחלקה להנדסה ביו-רפואית באוניברסיטת תל אביב המתמחה במניעה וטיפול בפצעי לחץ, חקר לאחרונה נזקים משמעותיים לעור כתוצאה משימוש בציוד מיגון אישי במיוחד מסכות פנים ומשקפי מגן – תועדו בקרב צוותים רפואיים המטפלים בחולי קורונה בכל העולם.
פצעים פתוחים בעור הפנים באנשי צוות רפואי מהווים פתח לזיהום על ידי חיידקים עמידים וכן וירוסים הנמצאים בסביבת בית החולים ובפרט, לחדירת נגיף הקורונה עצמו ישירות למחזור הדם. הפצעים הללו בעור הפנים הם למעשה סוג מסוים של פצעי לחץ הנגרמים כתוצאה משימוש במכשור וציוד רפואי, במקרה זה לא בחולים (כפי שהיה נפוץ עוד לפני מגפת הקורונה) אלא בצוות המטפל.
בקבוצתו של פרופ' עמית גפן במחלקה להנדסה ביו-רפואית שמומחיותו פצעי לחץ והגנה על הגוף מהפצעים הללו נחקר הנושא ופרסמו הנחיות מעשיות לצוותים רפואיים שמטרתן להפחית את הסיכון לפגיעה בעור כתוצאה משימוש בציוד מיגון אישי, למשל באמצעות הפחתת החיכוך על ידי סיכוך העור ושימוש בחבישות מגן.
מאמרו פורסם השבוע במגזין "Journal of Wound Care" והוא נגיש באופן חופשי מאתר המוציא לאור:
אלה שמתאהבים בבעיה הם אלה שממציאים לה פתרון

מחקר
ד"ר טלי אילוביץ מהמחלקה להנדסה ביו-רפואית באוניברסיטת תל אביב ביחד עם חוקרים מאוניברסיטת סטנפורד פיתחו טכנולוגיה לא פולשנית מבוססת אולטרסאונד לצורך העברת גנים אל תוך גידולים סרטניים

ד"ר טלי אילוביץ מהמחלקה להנדסה ביו-רפואית והעומדת בראש המעבדה לאולטרסאונד, מפתחת טכנולוגיות חדשות בתחום האולטרסאונד. דוגמא לטכנולוגיה שכזו היא שימוש באולטרסאונד טיפולי לצורך טיפולים לא פולשניים כתחליף להתערבות כירורגית חיצונית. הטיפול מושג ע"י שימוש בבועיות גז קטנות שקוטרן הוא כעשירית בלבד מקוטר תא דם אדום. במקור, הבועיות הללו פותחו כחומר ניגוד לדימות של כלי דם באולטרסאונד וכיום גם משמשות כפלטפורמה טכנולוגית לריפוי. באמצעות הזרקה של מיקרו-בועות ומיקוד של אולטרסאונד בתדר נמוך, הבועות תתכווצנה ותתרחבנה באזור הספציפי, דבר שיאפשר מעבר של חומרים מתוך כלי הדם אל הרקמה שמסביב. בצורה כזו לדוגמה ניתן להשתמש באולטרסאונד טיפולי שחודר מבעד לגולגולת כדי לפתוח את מחסום הדם-מוח בצורה ממוקדת והפיכה על מנת לאפשר מעבר של תרופות לטיפול במחלות שונות. את הפלטפורמה הזו ד"ר אילוביץ מקווה להמשיך לפתח ולהרחיב לטיפול במגוון מחלות, החל מגידולים סרטניים ועד לאלצהיימר ופרקינסון.
לאחר סיום הדוקטורט שלה, ד"ר אילוביץ המשיכה לפוסט דוקטורט בבית הספר לרפואה שבאוניברסיטת סטנפורד ובתחילת השנה הצטרפה לסגל המחלקה להנדסה ביו-רפואית באוניברסיטת תל אביב. במחקרה שהתפרסם החודש במגזין המדעי Proceedings of the National Academy of Sciences , ביחד עם חוקרים מאוניברסיטת סטנפורד פיתחו טכנולוגיה לא פולשנית מבוססת אולטרסאונד לצורך העברת גנים אל תוך גידולים סרטניים.
השיטה משלבת אולטרסאונד עם מיקרובועות שנקשרות אל התאים הסרטניים. כאשר אולטרסאונד מופעל, המיקרובועות מתנהגות כמו ראשי נפץ נקודתיים שיכולים לפעור חורים בממברנות של התאים הסרטניים ולאפשר מעבר של הגנים דרכם. הפלטפורמה הטיפולית החדשה נועדה לתפוס שתי ציפורים במכה אחת. ראשית, המיקרובועות תוקפות את התאים הסרטניים ולאחר מכן הגן שמועבר לתוכם מאותת למערכת החיסון להרוס את שארית הגידול. התגובה החיסונית המערכתית שנוצרת מסוגלת למגר גידולים נוספים שלא טופלו ישירות.
אלה שמתאהבים בבעיה הם אלה שממציאים לה פתרון